PERETA konsentrat 420mg/14ml N1
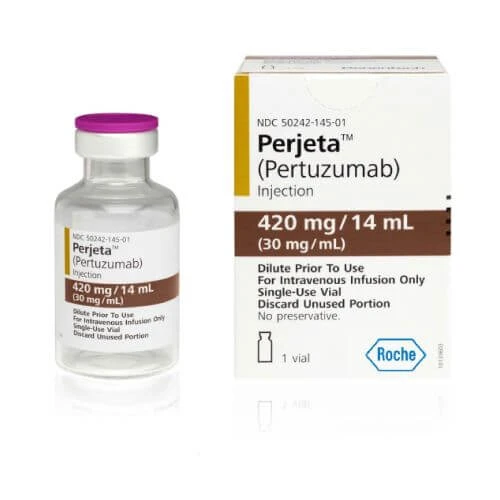
Mahsulotning ko'rinishi saytdagi rasmdan farq qilishi mumkin
Retseptli
Mahsulot haqida tafsilotlar
Ishlab chiqarilgan joyi:Germaniya
Kategoriya:O'smaga qarshi
Faol modda:pertuzumab
Ishlab chiqaruvchi:F. Hoffmann-La Roche Ltd, Shveysariya proizvedeno: Roche Diagnostics GmbH
ATX kodi:L01XC13
To‘lov va yetkazib berish usullari Toshkentda
Olib ketish
Ertaga yoki keyinroq 0 ta dorixonadan
Dorixonada karta yoki naqd to‘lov
Yetkazib berish
2 soat ichida yoki ertaga, yetkazib berish narxi onlayn dorixonada ko‘rsatilgan tarif bo‘yicha. Onlayn yoki kuryerga to‘lov
PERETA konsentrat 420mg/14ml N1 haqida qo'llanma
Diqqat: ushbu sahifadagi preparat tavsifi rasmiy yo‘riqnomaning soddalashtirilgan va to‘ldirilgan versiyasidir. Ma’lumot faqat tanishish maqsadida taqdim etilgan va o‘z-o‘zini davolash uchun qo‘llanma sifatida foydalanilmasligi kerak. PERETA konsentrat 420mg/14ml N1 preparatini qabul qilishdan oldin albatta shifokor bilan maslahatlashing
PERETA konsentrat 420mg/14ml N1 o'xshash dorilari

Buyuk Britaniya
Vakil:
«NOVATOR PHARMA», YaTT MChJIshlab chiqaruvchi:
«PRIMEA LIMITED»
Narxi
128 640 so'm dan
Narxi
544 000 so'm dan
Ruminiya
Ishlab chiqaruvchi:
S.C.Rompharm Company S.R.L.
Narxi
128 000 so'm dan
Narxi
1 150 000 so'm dan
Analoglar PERETA konsentrat 420mg/14ml N1
Analoglari yo'q
PERETA konsentrat 420mg/14ml N1 haqida savollar
PERETA konsentrat 420mg/14ml N1 haqida fikr-mulohazalar
Reyting 0, 0 ta sharh asosida